SSC 3rd Week Assignment Answer
বিষয়ঃ রসায়ন
বিষয় কোডঃ ১৩৭
অ্যাসাইনমেন্ট নম্বর-০২
অধ্যায় ও শিরােনামঃ চতুর্থ অধ্যায়: পর্যায় সারণি
এসাইনমেন্ট সপ্তাহঃ তৃতীয়
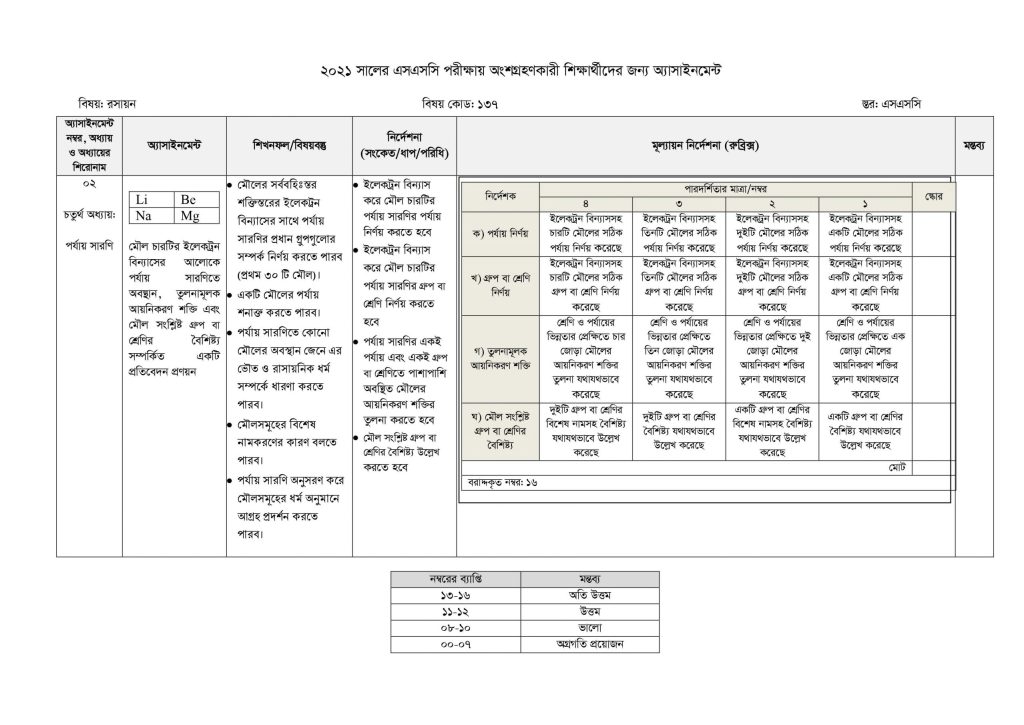
অ্যাসাইনমেন্টঃ
Li Na Be Mg মৌল চারটির ইলেকট্রন বিন্যাসের আলােকে পর্যায় সারণিতে অবস্থান, তুলনামূলক আয়নিকরণ শক্তি এবং মৌল সংশ্লিষ্ট গ্রুপ বা শ্রেণির বৈশিষ্ট্য সম্পর্কিত একটি প্রতিবেদন প্রণয়ন।
শিখনফল/বিষয়বস্তুঃ
- মৌলের সর্ববহিঃস্তর শক্তিস্তরের ইলেকট্রন বিন্যাসের সাথে পর্যায় সারণির প্রধান গ্রুপগুলাের সম্পর্ক নির্ণয় করতে পারব।
- (প্রথম ৩০ টি মৌল)। একটি মৌলের পর্যায় শনাক্ত করতে পারব।
- পর্যায় সারণিতে কোনাে মৌলের অবস্থান জেনে এর ভৌত ও রাসায়নিক ধর্ম সম্পর্কে ধারণা করতে পারব।
- মৌলসমূহের বিশেষ নামকরণের কারণ বলতে পারব।
- পর্যায় সারণি অনুসরণ করে মৌলসমূহের ধর্ম অনুমানে আগ্রহ প্রদর্শন করতে পারব।
নির্দেশনাঃ
- ইলেকট্রন বিন্যাস করে মৌল চারটির পর্যায় সারণির পর্যায় নির্ণয় করতে হবে।
- ইলেকট্রন বিন্যাস করে মৌল চারটির পর্যায় সারণির গ্রুপ বা শ্রেণি নির্ণয় করতে হবে।
- পর্যায় সারণির একই পর্যায় এবং একই গ্রুপ বা শ্রেণিতে পাশাপাশি অবস্থিত মৌলের আয়নিকরণ শক্তির তুলনা করতে হবে।
- মৌল সংশ্লিষ্ট গ্রুপ বা শ্রেণির বৈশিষ্ট্য উল্লেখ করতে হবে
রসায়ন তৃতীয় সপ্তাহের সমাধান
প্রতিবেদকের নামঃ
প্রতিবেদকের ঠিকানাঃ
প্রতিবেদনের তারিখঃ
Li Na Be Mg মৌল চারটির ইলেকট্রন বিন্যাসের আলােকে পর্যায় সারণিতে অবস্থান, তুলনামূলক আয়নিকরণ শক্তি এবং মৌল সংশ্লিষ্ট গ্রুপ বা শ্রেণির বৈশিষ্ট্য।
উদ্দীপকের মৌল ৪টি হলােঃ Li (3), Be (4), Na (11) ও Mg (12)
এদের ইলেকট্রন বিন্যাসঃ
Li (3): 1s² 2s¹
Be (4): 1s² 2s²
Na (11): 1s² 2s² 2p⁶ 3s¹
Mg (12): 1s² 2s² 2p⁶ 2s²
আমরা জানি, কোন মৌলের ইলেকট্রন বিন্যাসের বাইরের প্রধান শক্তিস্তরের নম্বর পর্যায় সংখ্যা এবং বাইরের প্রধান শক্তিস্তরে যদি শুধু s অরবিটাল থাকে তবে ঐ s অরবিটালের ইলেকট্রন সংখ্যাই গ্রুপ সংখ্যা।
SSC 3rd Week Assignment Answer রসায়ন তৃতীয় সপ্তাহের সমাধান
L এর পর্যায় সংখ্যা 2 এবং গ্রুপ নম্বর 1
Be এর পর্যায় সংখ্যা 2 এবং গ্রুপ নম্বর 2
Na এর পর্যায় সংখ্যা 3 এবং গ্রুপ নম্বর 1
Mg এর পর্যায় সংখ্যা 3 এবং গ্রুপ নম্বর 2
আয়নিকরণ শক্তিঃ
গ্যাসীয় অবস্থায় কোনাে মৌলের এক মােল গ্যাসীয় পরমাণু থেকে এক মােল ইলেকট্রন অপসারণ করে এক মােল ধনাত্মক আয়নে পরিণত করতে যে শক্তির প্রয়ােজন হয়, তাকে ঐ মৌলের আয়নিকরণ শক্তি বলে।
আমরা জানি, একই পর্যায়ের বামের মৌলের পারমাণবিক ব্যাসার্ধ বেশি এবং ডানের মৌলের পারমাণবিক ব্যাসার্ধ কম। আবার একই গ্রুপের উপরের মৌলের পারমাণবিক ব্যাসার্ধ কম এবং নিচের মোরে পারমাণবিক ব্যাসার্ধ বেশি।
পারমাণবিক ব্যাসার্ধ কমলে আয়নিকরণ শক্তির মান বাড়ে এবং পারমাণবিক ব্যাসার্ধ বাড়লে আয়নিকরণ শক্তির মান কমে।
Li ও Be, 2-নং পর্যায়ের যথাক্রমে 1-নং ও 2-নং গ্রুপে অবস্থিত। অর্থাৎ 2-নং পর্যায়ের বামদিকে Li ও ডানদিকে Be অবস্থিত। ফলে Li এর পারমাণবিক ব্যাসার্ধ বেশি এবং Be এর পারমাণবিক ব্যাসার্ধ কম।
সুতরাং Li এর আয়নিকরণ শক্তির মান কম এবং Be এর আয়নিকরণ শক্তির বেশি। অর্থাৎ আয়নিকরণ শক্তির ক্রম, Li < Be
Na ও Mg, 3-নং পর্যায়ের যথাক্রমে 1-নং ও 2-নং গ্রুপে অবস্থিত। অর্থাৎ 3-নং পর্যায়ের বামদিকে Na ও ডানদিকে Mg অবস্থিত। ফলে Na এর পারমাণবিক ব্যাসার্ধ বেশি এবং Mg এর পারমাণবিক ব্যাসার্ধ কম।
সুতরাং Na এর আয়নিকরণ শক্তির মান কম এবং Mg এর আয়নিকরণ শক্তির বেশি। অর্থাৎ আয়নিকরণ শক্তির ক্রম,
Na < Mg
আবার, Li ও Na, 1-নং গ্রুপের যথাক্রমে 2-নং ও3-নং পর্যায়ে অবস্থিত। অর্থাৎ 1-নং গ্রুপের উপরের দিকে Li ও নিচের দিকে Na অবস্থিত। ফলে Li এর পারমাণবিক ব্যাসার্ধ কম এবং Na এর পারমাণবিক ব্যাসার্ধ বেশি।
সুতরাং Li এর আয়নিকরণ শক্তির মান বেশি এবং Na এর আয়নিকরণ শক্তির মান কম। অর্থাৎ আয়নিকরণ শক্তির ক্রম’
SSC 3rd Week Assignment Answer রসায়ন তৃতীয় সপ্তাহের সমাধান
Li > Na
Be ও Mg, 2-নং গ্রুপের যথাক্রমে 2-নং ও 3-নং পর্যায়ে অবস্থিত। অর্থাৎ 2-নং গ্রুপের উপরের দিকে Be ও নিচের দিকে Mg অবস্থিত। ফলে Be এর পারমাণবিক ব্যাসার্ধ কম এবং Mg এর পারমাণবিক ব্যাসার্ধ বেশি।
সুতরাং Be এর আয়নিকরণ শক্তির মান। বেশি এবং Mg এর আয়নিকরণ শক্তির মান কম। অর্থাৎ আয়নিকরণ শক্তির ক্রম Be > Mg
অতএব প্রদত্ত মৌলসমূহের আয়নিক শক্তির তুলনা করলে পাই,
Be > Li > Mg > Na
8 মৌল সংশ্লিষ্ট গ্রুপ বা শ্রেণির বৈশিষ্ট্যঃ
প্রদত্ত মৌলগুলাের মধ্যে Li ও Na, 1-নং গ্রুপে এবং Be ও Mg, 2-নং গ্রুপে অবস্থিত।
গ্রুপ-1 এর বৈশিষ্ট্যঃ
গ্রুপ-1 এ 7টি মৌলের মধ্যে H ব্যতিত বাকি 6টি মৌলকে (Li, Na, K, Rb Cs, Fr) ক্ষারধাতু বলা হয়। অর্থাৎ গ্রুপ-1 ক্ষারধাতু নামে আখ্যায়িত করা হয়। এরা পানির সাথে বিক্রিয়া করে ক্ষার ও হাইড্রোজেন গ্যাস উৎপন্ন করে। যেমন, 2Na(s) + 2H2O (I) = 2NaOH (aq) + H2(g)
ক্ষারধাতুসমূহ 1-টি ইলেকট্রন ত্যাগ করে ক্যাটায়ন তৈরি করে। যেমন,
Na -e → Na+
- ক্ষারধাতুসমূহ নরম এবং এদের গলনাঙ্ক ও স্ফুটনাঙ্ক কম।
- পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে ক্ষারধাতুসমূহের পারমাণবিক ব্যাসার্ধ বৃদ্ধি পায়। ফলে আয়নিকরণ শক্তির মান কম হয়।
- ক্ষারধাতুসমূহ 1-টি ইলেকট্রন ত্যাগ করে ক্যাটায়ন তৈরি করে। এজন্য ক্ষারধাতুসমূহের জারণ সংখ্যা +1.
- ক্ষারধাতুসমূহ আয়নিক যৌগ গঠন করে। এদের যৌগসমূহ পানিতে দ্রবনীয়। এ যৌগগুলাে গলিত/দ্রবীভূত অবস্থায় বিদ্যুৎ পরিবাহী।
- পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে ক্ষারধাতুসমূহের সক্রিয়তা বৃদ্ধি পায়।
গ্রুপ-2 এর বৈশিষ্ট্যঃ
গ্রুপ-2 এ 6টি মৌল (Be, Mg, Ca, Sr, Ba, Ra) রয়েছে। এদেরকে মৃৎক্ষারধাতু বলা হয়। অর্থাৎ গ্রুপ-2 মৃৎক্ষারধাতু নামে পরিচিত। এই মৌলগুলােকে মাটিতে যৌগ হিসেবে পাওয়া যায় এবং পানির সাথে বিক্রিয়া করে ক্ষার উৎপন্ন করে।
যেমন, Mg(s) + 2H2O (1) = Mg(OH)2 (aq) + H2(g)
মৃৎক্ষারধাতুসমূহ 2-টি ইলেকট্রন ত্যাগ করে ক্যাটায়ন তৈরি করে।
SSC 3rd Week Assignment Answer রসায়ন তৃতীয় সপ্তাহের সমাধান
যেমন, Mg – 2e → Mg2+
- মৃৎক্ষার ধাতুসমূহের গলনাঙ্ক ও স্ফুটনাঙ্ক ক্ষারধাতুর তুলনায় বেশি।
- পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে মৃৎক্ষার ধাতুসমূহের পারমাণবিক ব্যাসার্ধ বৃদ্ধি পায়। ফলে আয়নিকরণ শক্তির মান কম হয়।
- ক্ষারধাতুসমূহ 2-টি ইলেকট্রন ত্যাগ করে ক্যাটায়ন তৈরি করে। এজন্য ক্ষারধাতুসমূহের জারণ সংখ্যা +2.
- ক্ষারধাতুসমূহ আয়নিক যৌগ গঠন করে। এদের যৌগসমূহ সাধারণত পানিতে দ্রবনীয়। এ যৌগগুলাে গলিত/দ্রবীভূত অবস্থায় বিদ্যুৎ পরিবাহী।
- পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে মৃৎক্ষার ধাতুসমূহের সক্রিয়তা বৃদ্ধি পায়।
জীবনবিজ্ঞান এসাইনমেন্ট তৃতীয় সপ্তাহ
বিষয়ঃ জীববিজ্ঞান
বিষয় কোডঃ ১৩৮
অ্যাসাইনমেন্ট নম্বর-০২
অধ্যায় ও শিরােনামঃ দ্বিতীয়; জীবকোষ ও টিস্যু
এসাইনমেন্ট সপ্তাহঃ তৃতীয়
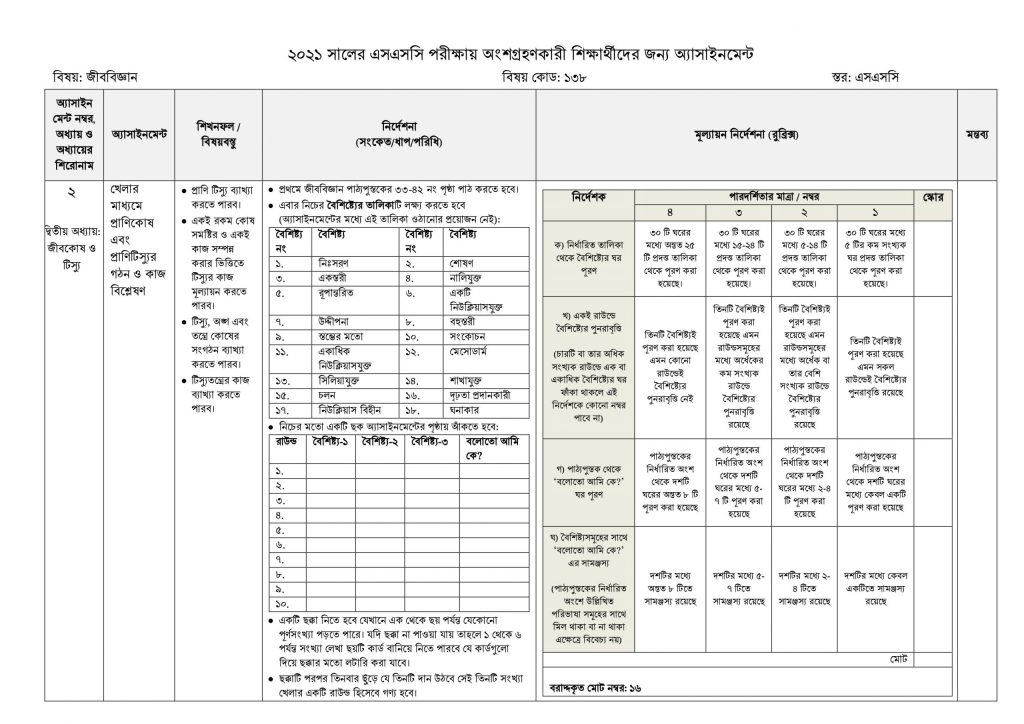
অ্যাসাইনমেন্টঃ
খেলার মাধ্যমে প্রাণী কোষ এবং প্রাণী কোষের গঠন ও কাজ বিশ্লেষণ।
শিখনফল/বিষয়বস্তুঃ
- প্রাণিটিস্যু ব্যাখ্যা করতে পারব।
- একই রকম করে সমষ্টিরও একই কাজ সম্পন্ন করার ভিত্তিতে টিস্যুর কাজ মূল্যায়ন করতে পারব।
- টিস্যু অঙ্গ এবং তন্ত্রের কোষের সংখ্যা গঠন ব্যাখ্যা করতে পারব।
- টিস্যুতন্ত্রের কাজ ব্যাখ্যা করতে পারব।
নির্দেশনাঃ
প্রথমে জীববিজ্ঞান পাঠ্যপুস্তকে 33-42 নং পৃষ্ঠা পাঠ করতে হবে।
এবার নিচের বৈশিষ্ট্য তালিকাটি লক্ষ করতে হবে।
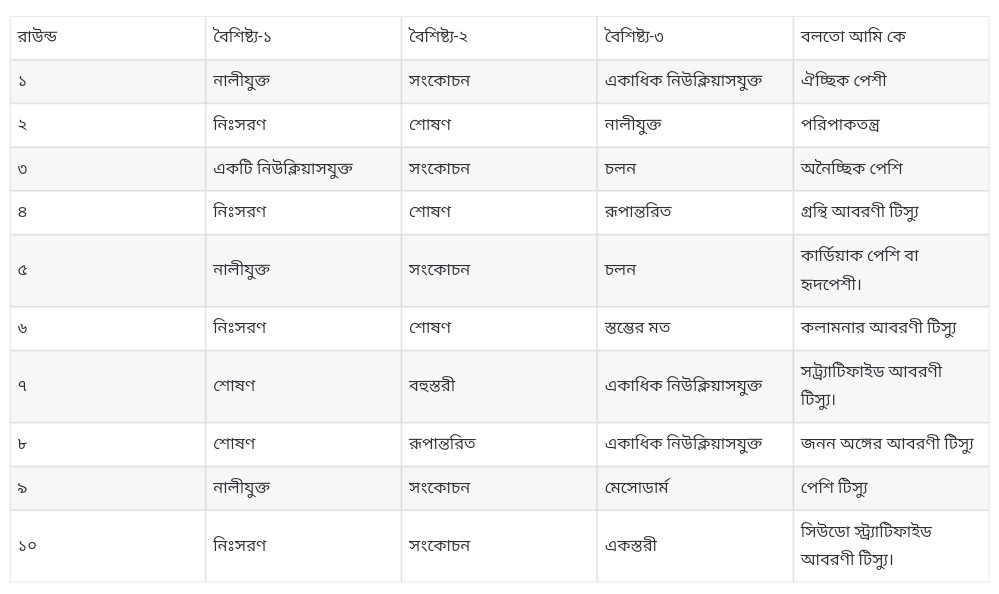
ছক্কাটি পরপর তিনবার সুরে যে তিনটি দান উঠবে সেই তিনটি সংখ্যা খেলার একটি রাউন্ড হিসেবে গণ্য হবে।
উদাহরণ: ধরা যাক, যথাক্রমে ৩, ৬ এবং ৪ পড়ল। তাহলে সেই রাউন্ডে উপরের বৈশিষ্ট্যের তালিকা থেকে বৈশিষ্ট্য-১ হিসেবে ৩ নং বৈশিষ্ট্য (একস্তরী) বেছে নিতে হবে;
বৈশিষ্ট্য-২ হিসেবে ৩+ ৬ = ১ নং বৈশিষ্ট্য (স্তম্ভের মতাে) বেছে নিতে হবে; এবং বৈশিষ্ট্য-৩ হিসেবে ৯+ ৪ = ১৩ নং বৈশিষ্ট্য (সিলিয়াযুক্ত) বেছে নিতে হবে।
ছকে নির্ধারিত ঘরে এগুলাে লিখতে হবে এবং বিলােতাে আমি কে?’ এর ঘরে ঐ তিনটি বৈশিষ্ট্য ধারণ করে এমন প্রাণিটিস্যু বা প্রাণিকোষের নাম লিখতে হবে।
SSC 3rd Week Assignment Answer
এই ঘর পূরণ করার জন্য অবশ্যই পাঠ্যপুস্তকে নির্ধারিত পৃষ্ঠাসমূহের (৩৩-৪২) মধ্যে থেকে মােটা হরফে ছাপা নামসমূহ বেছে নিতে হবে।
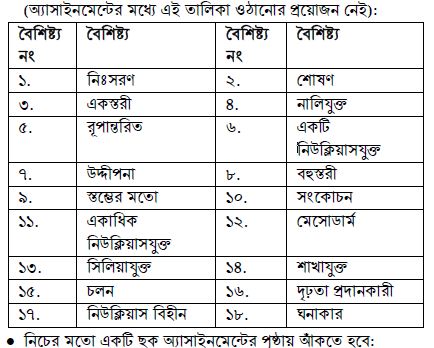
যদি সেই তিনটি বৈশিষ্ট্য মিলিয়ে কোনাে প্রাণিটিস্য বা প্রাণিকোষ না পাওয়া যায় তাহলে আবার ছক্কা ছুড়তে হবে এবং বৈশিষ্ট্য রাফ কাগজে নােট করতে হবে যতক্ষণ পর্যন্ত না এমন তিনটি বৈশিষ্ট্য পাওয়া যায় যেগুলাে দিয়ে একটি সত্যিকারের প্রাণিটিস্যু বা প্রাণিকোষ বােঝায়।
আমরা এসএসসি 2021 সালের পরীক্ষায় অংশগ্রহণকারী বিজ্ঞান বিভাগের জীববিজ্ঞান অ্যাসাইনমেন্ট এর তৃতীয় সপ্তাহের উত্তর নিচে তুলে ধরেছি।
ছাত্র-ছাত্রীরা প্রশ্ন বিশ্লেষণ করে আমাদের ওয়েবসাইটে প্রকাশিত উত্তরটি হুবহু সংগ্রহ করে পূর্ণাঙ্গ নম্বর পেতে পারেন। এখানে যেহেতু প্রাকটিক্যালি নিজেই উত্তর তৈরি করার জন্য বলা হয়েছে।
ছাত্র-ছাত্রীরা চাইলে আমাদের প্রকাশিত উত্তরে থেকে ধারণা নিয়ে নিজে নিজে প্রাক্টিক্যালি উত্তর তৈরি করে নিতে পারেন।
অন্যথায় আপনি সরাসরি নিজে প্রাক্টিক্যালি সব তৈরি করে আমাদের লিখিত উত্তরটি হুবহু কপি করে পরীক্ষায় পূর্ণ নম্বর পেতে পারেন।
এসএসসি ২০২১ সালের জীববিজ্ঞান দ্বিতীয় (তৃতীয় সপ্তাহ) অ্যাসাইনমেন্ট এর উত্তর নিচে দেওয়া হল।
SSC 3rd Week Assignment Answer রসায়ন তৃতীয় সপ্তাহের সমাধান
জীববিজ্ঞান তৃতীয় সপ্তাহের সমাধান
রাউন্ড-১
একটি ছক্কা পরপর ৩ বার ছুড়ে যে দান উঠলো তা হলো যথাক্রমে ৪, ৬, ১ তাহলে–
বৈশিষ্ট্য- ১ হবে ৪নং বৈশিষ্ট্য অর্থাৎ নালিযুক্ত
বৈশিষ্ট্য-২ হবে ৪+৬ = ১০নং বৈশিষ্ট্য অর্থাৎ সংকোচন
বৈশিষ্ট্য- ৩ হবে ১০ + ১ = ১১নং বৈশিষ্ট্য অর্থাৎ একাধিক নিউক্লিয়াসযুক্ত।
বৃত্তি, শিক্ষা, বিশ্ববিদ্যালয় ভর্তি পরীক্ষা, জাতীয় বিশ্ববিদ্যালয়, চাকরী, বিজ্ঞান ও প্রযুক্তি সহ সকল খবর সবার আগে পেতে আমাদের ওয়েবসাইটি নিয়মিত ভিজিট করুন।
Join Our Official Facebook Group
























Good